Abstract
La recente pubblicazione dei risultati clinici relativi all’impiego di Dostarlimab nel trattamento del carcinoma rettale localmente avanzato con instabilità dei microsatelliti (MSI-H) e deficit del sistema di riparazione del mismatch (dMMR) ha suscitato grande interesse nella comunità scientifica. Per la prima volta, una coorte di pazienti ha ottenuto una remissione completa della malattia mediante monoterapia immunologica, senza necessità di chirurgia, chemioterapia o radioterapia. Questo studio, pubblicato sul New England Journal of Medicine, rappresenta un potenziale punto di svolta nella terapia oncologica, dimostrando la possibilità di trattamenti personalizzati, meno invasivi e con un profilo di tollerabilità nettamente superiore rispetto alle terapie convenzionali. Il presente articolo analizza i fondamenti biologici dell’immunoterapia con inibitori di PD-1, illustra i risultati dello studio su Dostarlimab, confronta i benefici rispetto ai trattamenti oncologici tradizionali e riflette sulle prospettive future di questa strategia terapeutica emergente.
Per decenni, la lotta contro le neoplasie si è basata su tre pilastri terapeutici: chemioterapia, radioterapia e chirurgia. Sebbene tali strategie abbiano determinato importanti successi in termini di sopravvivenza, esse sono gravate da significativi limiti: elevata tossicità sistemica, scarsa selettività cellulare e impatto sostanziale sulla qualità della vita dei pazienti.
Negli ultimi anni, tuttavia, si è assistito a una trasformazione radicale del panorama terapeutico oncologico, grazie all’emergere delle immunoterapie. Tra queste, il farmaco Dostarlimab ha attirato l’attenzione della comunità scientifica per i risultati straordinari ottenuti in uno studio clinico condotto su pazienti affetti da tumore rettale localmente avanzato con deficit di riparazione del mismatch (dMMR).
Contenuti
- 1. I limiti intrinseci delle terapie oncologiche tradizionali
- 2. Immunoterapia e targeting dei checkpoint: un approccio innovativo
- 3. Il caso Dostarlimab: remissione completa senza trattamento convenzionale
- 4. Implicazioni cliniche e benefici terapeutici
- 5. Considerazioni critiche: limiti e prospettive
- 6. Prospettive future
- Conclusione
1. I limiti intrinseci delle terapie oncologiche tradizionali
- Chemioterapia. La chemioterapia si fonda sull’utilizzo di agenti citotossici non selettivi che colpiscono preferenzialmente le cellule a rapida proliferazione, indipendentemente dalla loro natura neoplastica o fisiologica. Ciò comporta una vasta gamma di effetti collaterali: mielosoppressione, alopecia, nausea, vomito, mucositi e immunosoppressione generalizzata. Inoltre, nei tumori recidivanti si osserva frequentemente lo sviluppo di farmacoresistenza.
- Radioterapia. Analogamente, la radioterapia, pur essendo localizzata, induce danni collaterali ai tessuti sani adiacenti alla massa tumorale. I rischi includono fibrosi, necrosi tissutale, infiammazione cronica e, in alcuni casi, la genesi di tumori secondari radioindotti, dovuti agli effetti mutageni delle radiazioni ionizzanti.
2. Immunoterapia e targeting dei checkpoint: un approccio innovativo
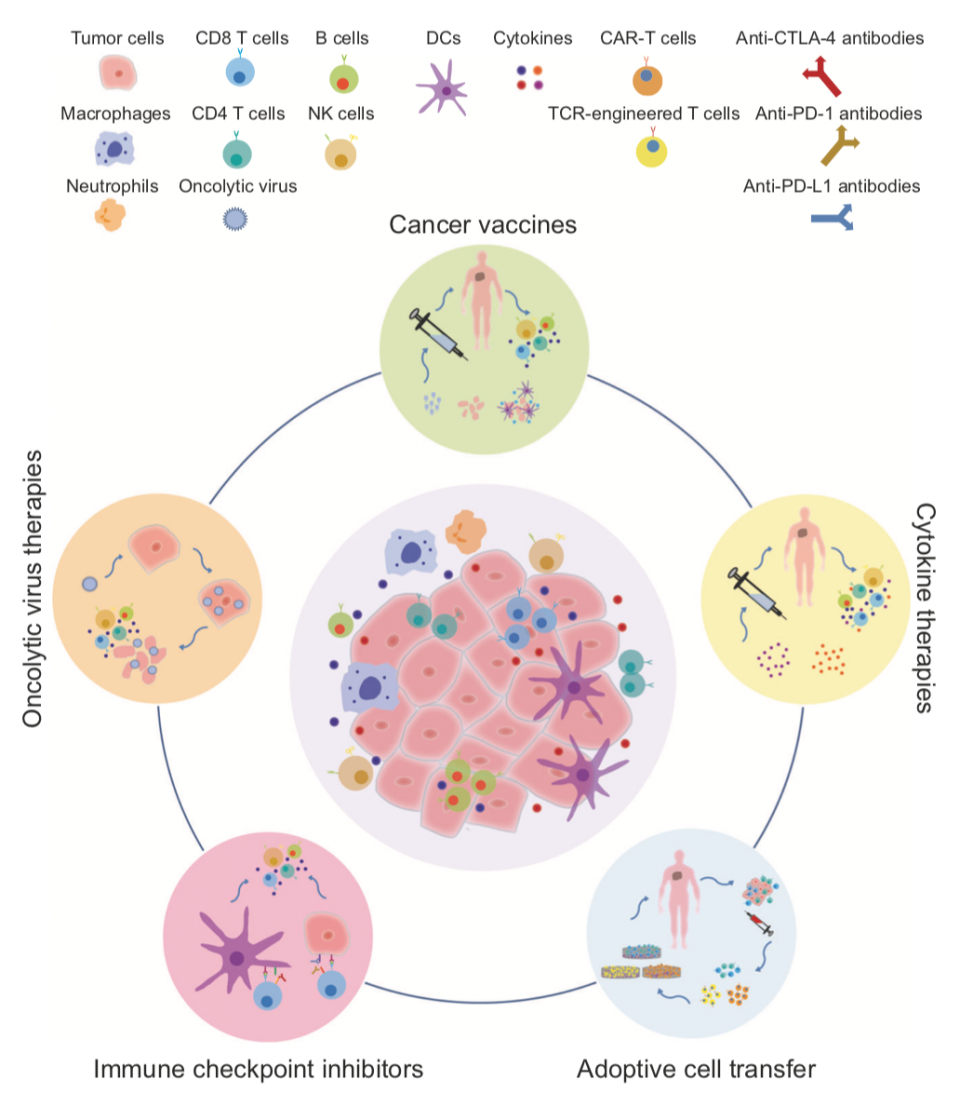
La scoperta dei checkpoint immunitari ha segnato una svolta epocale nella comprensione dell’immuno-evasione tumorale. Molecole come PD-1, PD-L1 e CTLA-4 agiscono da freni fisiologici del sistema immunitario; tuttavia, molte neoplasie ne sfruttano l’espressione per sfuggire al controllo dei linfociti T citotossici.
I farmaci inibitori dei checkpoint immunitari (immune checkpoint inhibitors, ICI) bloccano tali meccanismi di inibizione, ripristinando la capacità del sistema immunitario di riconoscere e distruggere le cellule tumorali. Questo approccio, più selettivo e meno citotossico, si è dimostrato capace di indurre remissioni durature in una quota significativa di pazienti con tumori avanzati.
3. Il caso Dostarlimab: remissione completa senza trattamento convenzionale
Nel giugno 2022, uno studio pubblicato sul New England Journal of Medicine (Cercek et al.) ha riportato i risultati di una sperimentazione clinica condotta su 12 pazienti affetti da adenocarcinoma rettale localmente avanzato con deficit di riparazione del mismatch (dMMR).
Tutti i pazienti sono stati trattati esclusivamente con Dostarlimab, un anticorpo monoclonale umanizzato diretto contro il recettore PD-1. L’inibizione di tale checkpoint ha consentito al sistema immunitario di eliminare le cellule tumorali senza ricorso ad alcuna forma di trattamento convenzionale (chemio, radio o chirurgia).
Tutti i pazienti hanno raggiunto una risposta clinica completa, documentata mediante imaging e biopsia, con assenza di recidiva a un follow-up mediano di dodici mesi.
4. Implicazioni cliniche e benefici terapeutici
| Aspetto | Vantaggio osservato |
|---|---|
| Selettività biologica | Il farmaco agisce solo in presenza di biomarcatori specifici (dMMR/MSI-H) |
| Minore tossicità | Assenza di mielosoppressione, alopecia o disturbi gastrointestinali severi |
| Preservazione funzionale | Nessun danno alla funzionalità ano-rettale, preservata l’integrità anatomica |
| Qualità della vita | Drastico miglioramento rispetto agli effetti collaterali delle terapie standard |
| Potenziale durabilità | Risposte immunologiche prolungate grazie alla memoria linfocitaria |
5. Considerazioni critiche: limiti e prospettive
Nonostante l’entusiasmo, è opportuno mantenere una prospettiva rigorosa e scientificamente cauta. Lo studio iniziale ha coinvolto un numero molto limitato di pazienti e con un tempo di follow-up ancora insufficiente per valutare pienamente la durabilità delle remissioni o l’eventuale insorgenza di metastasi a lungo termine.
Inoltre, l’applicabilità di Dostarlimab è per ora circoscritta a una sottopopolazione tumorale ben definita: i tumori con instabilità dei microsatelliti o deficit di mismatch repair, che rappresentano una minoranza nei carcinomi rettali (circa il 5-10%).
Vi sono poi considerazioni economiche non trascurabili: il costo dei farmaci immunoterapici resta elevato, e l’accessibilità non è ancora universale nei sistemi sanitari pubblici.
6. Prospettive future
Il successo di Dostarlimab ha stimolato nuove ricerche su altri tipi di tumore caratterizzati da MSI-H o dMMR, come l’endometrio, l’ovaio, il polmone e il melanoma. Sono attualmente in corso studi clinici che esplorano il potenziale combinatorio della molecola con altri agenti target (come PARP-inibitori o vaccini neoantigenici).
Parallelamente, il sequenziamento genomico tumorale si sta imponendo come strumento diagnostico imprescindibile per identificare i pazienti eleggibili all’immunoterapia.
Conclusione
L’utilizzo di Dostarlimab nei tumori dMMR rappresenta un progresso concreto verso una medicina oncologica più personalizzata, immuno-mediata e meno invasiva. Sebbene non si tratti di una terapia universale, questo approccio dimostra come, in sottogruppi selezionati, sia possibile ottenere remissioni complete senza dover ricorrere ai trattamenti convenzionali, aprendo prospettive nuove e più umane nella gestione del cancro.
Se confermati su larga scala, questi risultati potrebbero segnare un punto di svolta nella storia della terapia oncologica.
Riferimenti bibliografici
- Cercek, A., et al. (2022). PD-1 Blockade in Mismatch Repair–Deficient, Locally Advanced Rectal Cancer. New England Journal of Medicine, 386(26), 2363-2376. DOI: 10.1056/NEJMoa2201445
- Stadler, Z. K., & Cercek, A. (2024). PD-1 blockade in dMMR/MSI-H locally advanced rectal cancer: A new standard of care? Seminars in Oncology, 51(2), 151602. DOI: 10.1016/j.seminoncol.2024.151602




